Coronavirus in Deutschland
Faktencheck nach AfD-Behauptung: Zweifelt Biontech wirklich am eigenen Impfstoff?
Stand 09.05.22 - 11:58 Uhr
0
Mit Verweis auf ein internes Dokument wird dem Impfstoff-Hersteller Biontech unterstellt, er sei selbst gar nicht überzeugt von seinem Corona-Präparat. Was ist dran an der AfD-Behauptung? Ein Faktencheck.
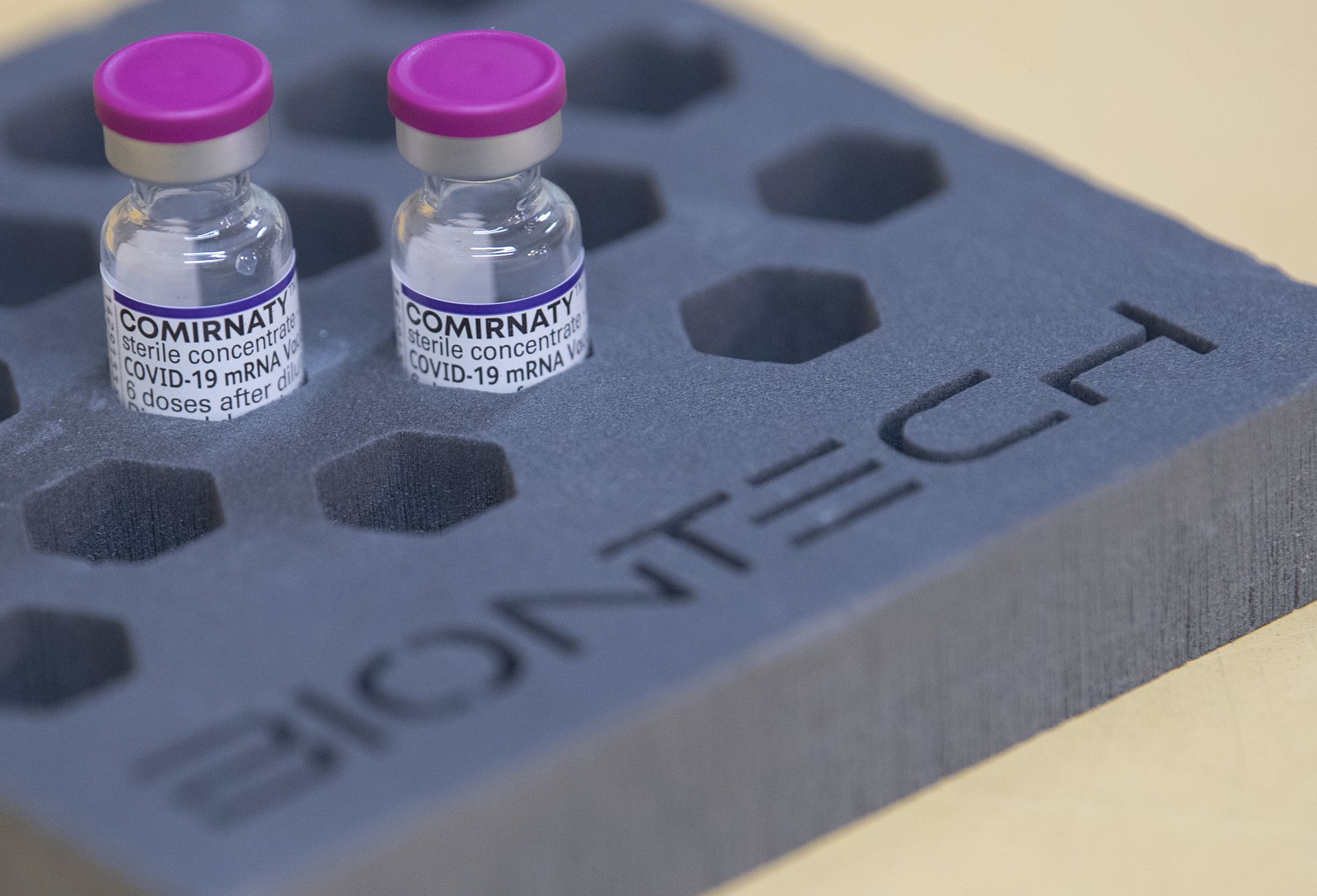
Nach aktuellem Stand der Wissenschaft hat Comirnaty bei Infektion mit der Delta-Variante eine Wirksamkeit von etwa 90 Prozent gegen eine schwere Covid-19-Erkrankung – bei der Omikron-Mutante zeigen erste Daten, dass der Schutz weniger gut ist.
Was steckt hinter der AfD-Behauptung?
Seit fast anderthalb Jahren wird der Impfstoff von Biontech weltweit gegen das Coronavirus eingesetzt. Millionen Menschen bietet er Schutz gegen schwerwiegende Covid-Erkrankungen. Obwohl das bereits viele internationale Untersuchungen nachgewiesen haben, laufen Impfgegner weiter Sturm gegen das Mittel.
- Anzeige -
Jüngst wird mit Verweis auf ein Biontech-Dokument aus den USA dem Hersteller unterstellt, er selbst sei gar nicht überzeugt von seinem Impfstoff.
Was ist an der Behauptung dran?
Behauptung: «Biontech glaubt nicht mal selbst an die Impfung», heißt es etwa von der AfD.
Bewertung: Falsch.
Fakten: Im Mittelpunkt des Vorwurfs in Richtung des Pharmaunternehmens aus Mainz steht dessen Bericht an die US-Börsenaufsicht SEC (Securities and Exchange Commission) vom 30. März 2022 über das Geschäftsjahr 2021. Ein solcher muss nach dem US-Handelsgesetz jährlich von ausländischen Aktiengesellschaften vorgelegt werden.
Grundsätzlich verweist Biontech in diesem Bericht auf das «hohe Schutzniveau» der Impfung. Das Mittel biete «ein hohes Maß an Schutz gegen bedenkliche Varianten, einschließlich Alpha, Beta und Delta». Jüngste Laborstudien hätten zudem gezeigt, dass drei Impfdosen auch gegen die Variante Omikron wirkten, so das Unternehmen.
Doch vor allem ein Satz im insgesamt 700 Seiten umfassenden Papier erhitzt die Gemüter. Biontech schreibt: «Es könnte sein, dass wir nicht in der Lage sind, eine ausreichende Wirksamkeit oder Sicherheit unseres Covid-19-Impfstoffs und/oder variantenspezifischer Präparate nachzuweisen, um eine dauerhafte behördliche Zulassung in den USA, in Großbritannien, in der Europäischen Union oder in anderen Ländern zu erhalten, in denen der Impfstoff eine Notzulassung oder eine bedingte Marktzulassung erhalten hat.»
Einige schließen daraus, dass selbst der Hersteller einräumt, ein unwirksames und unsicheres Mittel auf den Markt gebracht zu haben.
Börsenaufsicht macht genaue Vorschriften
Doch das stimmt nicht. Die Aussage fällt in einem Warnhinweis mit Vorhersagen der Geschäftsführung («Cautionary statement regarding forward-looking statements»). Diese juristischen Angaben sind von der Börsenaufsicht detailliert vorgeschrieben, um mögliche Schadenersatzklagen von Investoren zu vermeiden.
Im Biontech-Bericht führt diese Vorschrift dazu, dass alle denkbaren Einflüsse auf den Unternehmensgewinn und die geschäftliche Entwicklung geschildert werden müssen. Damit sollen sich Investoren über sämtliche möglichen Risiken ein Bild machen können.
Zu den aufgeführten potenziellen Unwägbarkeiten gehört unter anderem auch die Konkurrenz durch andere Impfstoffe und deren Effizienz, Kosten, Transport- und Lagermöglichkeiten, Sicherheit, Nebenwirkungen und Beständigkeit der Immunantwort. Die Geschäftsergebnisse könnten auch beeinflusst werden, etwa durch «das Ausmaß, in dem ein Covid-19-Vakzin in der Zukunft weiterhin nötig sein wird».
Derzeit gilt für den Biontech-Impfstoff Comirnaty in der Europäischen Union eine bedingte Marktzulassung. Diese wurde erstmals im Dezember 2020 erteilt und im November 2021 um ein weiteres Jahr verlängert.
- Anzeige -
Wie sich Comirnaty in Studien geschlagen hat
An die Sicherheit von Covid-19-Impfstoffen werden von der Europäischen Arzneimittel-Agentur (EMA) dieselben Anforderungen gestellt wie an jeden anderen in der EU zugelassenen Impfstoff. Bei einer bedingten Zulassung werden Daten bewertet, sobald sie verfügbar sind – und nicht erst, wenn alle Untersuchungen abgeschlossen sind.
Nach einer anfänglichen Notfallzulassung in den USA hatte die Arzneimittelbehörde FDA dem Mittel bereits im August 2021 die vollständige Zulassung erteilt.
Nach aktuellem Stand der Wissenschaft hat Comirnaty bei Infektion mit der Delta-Variante eine Wirksamkeit von etwa 90 Prozent gegen eine schwere Covid-19-Erkrankung. Bei der Omikron-Mutante zeigen erste Daten nach Angaben des Robert Koch-Instituts, dass der Schutz weniger gut ist.
In einer von Pfizer finanzierten Studie betrug die Wirksamkeit nach drei Dosen gegen Krankenhauseinweisungen wegen Omikron 85 Prozent innerhalb der ersten drei Monate nach der Impfung. Sie fiel aber auf 55 Prozent nach drei Monaten oder länger. Zu keinem Zeitpunkt in der Pandemie haben namhafte Forscher behauptet, eine Corona-Impfung schütze zu 100 Prozent vor Covid-19.
Mit Material der dpa
Mehr Beiträge und Themen
Schockierende Videos sind aus der Hundestagesstätte Isarpfoten e.V. aufgetaucht: Ein oder mehrere Mitarbeitende werden dabei gezeigt, wie sie Hunde quälen.
Wegen des heftigen Schneefalls am Wochenende und den anhaltend schlechten Straßenverhältnissen, fällt an einigen Orten in Bayern die Schule aus. Hier gibt's die aktuelle Übersicht.
Die Schneemassen haben München weiterhin im Griff - und das merkt man auch im Nahverkehr. Auswirkungen gibt es zum Teil noch bei der Regionalverkehr mit Zügen und den Trambahnen.
Albtraum Flughafen: Nach den kräftigen Schneefällen des Wochenendes ist der Flugverkehr in München nach wie vor stark eingeschränkt. Hunderte Passagiere stecken fest. Auch für Dienstag ist keine Normalisierung in Sicht.
Schnee und Eis sorgen in Süddeutschland weiter für Verkehrsprobleme. Vielerorts fahren im Süden Bayerns auch zwei Tage nach den massiven Schneefällen noch keine Züge; Flüge fallen aus - eine komplette Rückkehr zum «Normal» wird noch dauern.
95.5 Charivari schickt dich auf Münchens größte Silvesterparty: SOMNIA im Zenith. Wir laden dich und deine Freunde auf eine legendäre Silvesternacht ein, hier gibt’s alle Infos!
Winter in München - doch die Arbeit macht keine Pause. Was ist, wenn ich wegen des Schneechaos nicht rechtzeitig zu meinem Job erscheine? Droht mir eine Abmahnung?
Das Wochenende war in München aufgrund des Schneetreibens ziemlich chaotisch. Ein paar Einschränkungen bleiben auch noch unter der Woche.
Schneemassen am Wochenende in Süddeutschland sorgten für Verkehrschaos und Stromausfälle. Die Auswirkungen sind noch deutlich spürbar.
Die Christkindlmarkt-Saison in München Stadt und Land läuft. Auf welche du dich freuen kannst, zeigen wir dir hier.
In einem aktuell festgefahrenen Tarifkonflikt baut die GDL mit dem nächsten Warnstreik weiter Druck auf. Worauf sich die Fahrgäste einstellen müssen - jetzt und im neuen Jahr.
Der Münchner Nahverkehr soll einfacher, größer und besser werden. Zum Dezember gibt es schon erste Änderungen durch die Gebietserweiterung.
Wer bei einem Arzt bereits bekannt ist und keine schweren Krankheitssymptome hat, kann sich künftig wieder telefonisch krankschreiben lassen.
Die Polizei sucht nach einem 69-Jährigen, der vermisst wird und auf Hilfe angewiesen ist. Wer hat ihn gesehen?
Die Lokführer treten in den Streik - ab Donnerstagabend bis Freitagabend. Die GDL übt damit weiter Druck auf die Deutsche Bahn aus.
Der Stadtrat hat den Mietenstopp für städtische Wohnungen offiziell bestätigt - und das unbefristet. Betroffen sind rund 170.000 Münchner.
An Bayerns Schulen soll das Gendern verboten werden. So will es der Ministerpräsident. In der gerne zitierten Schulfamilie kommt Söders Vorstoß alles andere als gut an.















